Московский научно-исследовательский клинический институт им. М.Ф. Владимирского, Институт морфологии человека РАМН, Москва
Л.Е. Гуревич
Для определения гистогенеза разных типов опухолей используют современные методы диагностики – иммуногистохимический (ИГХ), электронно-микроскопический, молекулярно#биологический (гибридизация in situ), генетический, которые позволяют более полно охарактеризовать биологический потенциал опухолевых клеток.
Эндокринные или нейроэндокринные опухоли (НЭО) могут возникать в любых органах, где в норме имеются эндокринные клетки: в желудочно-кишечном тракте (ЖКТ), легких, тимусе, почках, яичниках, предстательной, молочной и щитовидной железах, коже. НЭОЖКТ редкие и обычно медленно растущие новообразования, при которых существенное ухудшение качества жизни пациентов даже при наличии метастазов происходит на поздней стадии болезни. Опухоли чаще бывают клинически нефункционирующими, а в случае функционирующих развиваются гиперфункциональные эндокринные синдромы, угрожающие жизни пациентов.
В литературе и клинической практике для обозначения НЭОЖКТ до сих пор используют несколько синонимов. Обендорфер в 1907 г предложил термин «карциноид» для обозначения интестинальных опухолей с менее агрессивным, чем у аденокарцином, клиническим течением. Эндокринная природа этих опухолей была доказана Мерлингом в 1938 г В настоящее время термин «карциноид» применяют только для НЭОЖКТ, которые вызывают карциноидный синдром и клетки которых продуцируют серотонин, гистамин, тахикинин, простагландин и другие пептидные гормоны. В 1964 г. Пирс предложил для таких опухолей термин АПУД-ома на основании гипотезы об общем нейроэктодермальном происхождении эндокринных клеток ЖКТ, общим свойством которых, как он полагал, является способность утилизировать и декарбоксилировать предшественники аминов. В дальнейшем было доказано, что все эндокринные клетки ЖКТ происходят от общих стволовых клеток-предшественниц. Термином «островково-клеточные опухоли» часто обозначают эндокринные опухоли поджелудочной железы (ПЖ), хотя он не подходит для опухолей, секретирующих гормоны, в норме не вырабатываемые клетками эндокринных островков (например, гастрин, АКТГ, ВИП и некоторые другие) (табл. 1). Классификация TNM, которая успешно используется для определения стадии других типов опухолей, для НЭО не подходит, как не пригодны для прогноза их злокачественности и два важных морфологических критерия - клеточная и ядерная атипия (за исключением мелкоклеточной нейроэндокринной карциномы).
В настоящее время для определения гистогенеза разных типов опухолей используют современные методы диагностики - иммуногистохимический (ИГХ), электронно-микроскопический, молекулярно-биологический (гибридизация in situ), генетический, которые позволяют более полно охарактеризовать биологический потенциал опухолевых клеток. Наиболее распространенные в современной литературе термины «нейроэндокринная опухоль» и «нейроэндокринная карцинома» базируются на наличии у всех эндокринных (нейроэндокринных) клеток ЖКТ общих иммунофенотипических особенностей. Предварительный диагноз НЭО может быть поставлен на основании клинической картины и обычного гистологического исследования, а окончательная верификация проводится с помощью ИГХ-исследования. Клетки НЭО дают положительную реакцию с антителами к общим нейроэндокринным маркерам - хромогранину А (маркеру специфических эндокринных гранул), синаптофизину (маркеру мелких везикул с нейротрансмиттерами), CD56 (маркеру молекул нейроадгезии), NSE и PGP 9,5 (маркерам цитоплазматических протеинов - нейронспецифической энолазе и протеину генного продукта 9,5). Для того, чтобы установить тип НЭО, используют специфические эндокринные маркеры - пептиды и/или амины, обладающие активностью гормонов (инсулин, глюкагон, соматостатин, вазоактивный интестинальный полипептид, панкреатический полипептид, гастрин, серотонин, АКТГ, кальцитонин, и другие). НЭО часто продуцируют несколько гормонов, поэтому диагноз базируется как на наличии характерного гиперфункционального синдрома, так и на выявлении доминирующей популяции эндокринных клеток, которая составляет не менее 50% всех клеток опухоли. В соответствии с этим НЭО верифицируют как инсулиномы, глюкагономы, гастриномы, соматостатиномы, пипомы, випомы, кальцитониномы, карциноиды и др. Важная информация о функциональном статусе опухоли может быть получена при исследовании ультраструктуры опухолевых клеток. Тип эндокринных гранул и их количество позволяют уточнить диагноз НЭО. Например, в нормальных В-клетках и клетках доброкачественных инсулином имеется большое число p-гранул с кристаллоидным ядром, способных депонировать инсулин, а в клетках злокачественных и менее дифференцированных - увеличивется количество p-гранул с округлым ядром или атипиных, в которых секретируется проинсулин и которые не способны длительно хранить гормон и спонтанно выделяют его в кровеносное русло.
Таблица №1.
Классификация и основные симптомы эндокринных опухолей желудочно-кишечного тракта
| Синдром | Основные симптомы | Основной гормон | Другие гормоны | Степень злока-чествен-ности (%) | Локали-зация | Экстра-
панкреати-
ческая локализация |
| Инсулинома | Гипогликемия | Инсулин | Глюкагон, ПП | 5-10 | ПЖ | Очень редко |
| Гастринома (синдром Золлингера-Эллиссона) | Пептические язвы, диарея, рефлюксная болезнь | Гастрин | Инсулин, ПП, глюкагон, АКТГ, соматостатин | >90 | ПЖ | Двенадцати-перстная кишка, желудок, брыжейка |
| Карциноидный синдром | Приливы, диарея, бронхиальная обструкция | Серотонин | Тахикинин, простагландин, хромогранин А | 100 | Кишечник | ПЖ (редко) |
| ВИПома (синдром Вернера - Моррисона) - панкреатическая холера | Стойкая диарея, гипокалиемия | ВИП, PHI | ПП, глюкагон, соматостатин, хромогранин А | 75-100 | ПЖ | |
| Глюкагонома | Некролитическая мигрирующая эритема, диабет | Глюкагон | ПП, инсулин, соматостатин, хромогранин А | 50 | ПЖ | Редко |
| Соматостатинома | Диабет, стеаторея, жёлчнокаменная болезнь | Соматостатин | ПП, инсулин, кальцитонин | 50 | ПЖ | Двенадцати-перстная кишка |
| GHRH-ма | Акромегалия | GHRH | Соматостатин, гастрин, инсулин | 100 | ПЖ | Легкие |
| CRH-ома, АКТГ-ома | Синдром Кушинга | CRH, АКТГ | Гастрин, ПП, хромогранин А | >90 | ПЖ | Легкие |
Примечание: АКТГ - адренокортикотропный гормон; CGH - кортикотропин-рилизинг-гормон; GHRH - гормон роста-рилизинг-гормон; PHI - пептид гистидин изолейцин; ПП - панкреатический полипептид; ВИП - вазоактивный интестинальный пептид.
В основе прежних классификаций НЭОЖКТ лежали клинические проявления, что не отражало полиморфизма этих опухолей. В 2000 г ВОЗ была разработана новая классификация НЭОЖКТ [19], которая делит их в соответствии с локализацией, клиническими проявлениями, степенью дифференцировки и биологическим потенциалом опухолевых клеток, прогнозом (табл. 1).
Нейроэндокринные опухоли пищевода встречаются очень редко и составляют примерно 0,05% всех НЭОЖКТ. Они обычно крупные (>4 см), локализуются в дистальном отделе пищевода и не дают специфических гормональных синдромов. Опухоли представлены двумя гистологическими типами: в виде солидных комплексов высокодифференцированных клеток и мелко- или крупноклеточными эндокринными карциномами, аналогичными соответствующим опухолям легких. Еще реже встречаются смешанные экзо-эндокринные карциномы. Прогноз зависит от степени дифференцировки опухолевых клеток и от стадии опухоли [3, 14].
Нейроэндокринные опухоли поджелудочной железы (НЭОПЖ) составляют большинство функционирующих НЭОЖКТ (табл. 2).
НЭОПЖ имеют трабекулярное, альвеолярное, солидное, псевдожелезистое, анигиоматозное, ациноподобное и другие типы строения. Разнообразны они и по функциональной активности и спектру продуцируемых гормонов. Большинство относят к высокодифференцированным доброкачественным опухолям, но имеется группа новообразований неопределенной степени злокачественности, определение биологического потенциала которых до сих пор является сложной диагностической проблемой [1-4, 10, 11, 15, 19]. Самыми надежными гистологическими критериями злокачественности НЭОПЖ является инвазия кровеносных и лимфатических сосудов и нейроинвазия, которые встречаются в 90% опухолей с метастазами или массивной инвазией и лишь в 30% опухолей без метастазов и без инвазии окружающих тканей. Опухоли чаще всего метастазируют в печень и лимфатические узлы (парапанкреатические, ворот печени, парааортальные, мезентериальные), в редких случаях - в лимфатические узлы средостения и подмышечные, еще реже в кости, брюшину, легкие, почки, щитовидную железу. Опухоли, которые обычно локализуются в теле и хвосте ПЖ (глюкагономы, инсулиномы, випомы), имеют склонность к гематогенной диссеминации, а гастриномы чаще метастазируют в лимфатические узлы. Опухоли, продуцирующие островковые гормоны (инсулин, глюкагон, соматостатин и РР), обычно менее злокачественные (в 10-20%), чем те, которые продуцируют кишечные или эктопические гормоны (гастрин, ВИП, нейротензин, АКТГ, гормон роста - в 60-80%). В новой классификации предложены следующие критерии малигнизации НЭОПЖ (в порядке убывающей значимости): метастазы, макроскопически видимая местная инвазия, инвазия периневральных пространств и кровеносных сосудов, размеры опухоли более 3 см.
Таблица №2.
Классификация эндокринных опухолей поджелудочной железы [4, 19]
1. Высокодифференцированные эндокринные опухоли.
1.1. Доброкачественные: локализованы в пределах ПЖ, без сосудистой инвазии, размером 2 см и менееа, с числом митозов 0-2 на 10 на РПЗ, 0-2% Ki-67-позитивных клеток.
1.1.1. Функционирующие - инсулиномы.
1.1.2. Нефункционирующие.
1.2. Опухоли неопределенной степени злокачественности: локализованы в пределах ПЖ, без сосудистой инвазии, размером >2 сма или с эктопическим синдромом, с более 2 митозами на 10 РПЗ и >2% Ki-67-позитивных клеток.
1.2.1. Функционирующие - гастринома, инсулинома, випома, глюкагонома, соматостатинома или с эктопическим синдромомь.
1.2.2. Нефункционирующие |
2. Высокодифференцированные эндокринные карциномы: низкой степени злокачественности с выраженной локальной инвазией и/ или метастазами.
2.1. Функционирующие - гастринома, инсулинома, глюкагонома, випома, соматостатинома или с эктопическим синдромомь.
2.2. Нефункционирующие. |
| 3. Низкодифференцированные мелкоклеточные эндокринные карциномы высокой степени злокачественности. |
Примечание: а - опухоли размером менее 2 см доброкачественны почти в 100% случаев, менее 3 см - почти в 90%.случаев; b - эктопические синдромы: синдром Кушинга (АКТГ), акромегалии или гигантизма (гормон роста), гиперкальциемии и т.д. РПЗ - репрезентативные поля зрения.
Доброкачественные опухоли обычно состоят из клеток мелких и средних размеров со слабо или умеренно выраженной атипией. Высокодифференцированные эндокринные карциномы низкой степени злокачественности чаще имеют более крупные размеры (более 3 см), капсула опухоли отсутствует или неполная, инвазия крупных сосудов или отдаленные метастазы не характерны. Преобладают участки «диффузного» или солидного строения, которые часто чередуются с участками из крупных, плохо очерченных трабекул, мелких цепочек и цугов, замурованных в обильной гиалинизированной или плотной фиброзной строме. Для них характерна слабо или умеренно выраженная клеточная атипия, гиперхромность ядер с выраженными ядрышками, увеличение ядерно-цитоплазматического отношения, митотическая активность до 2-10 митозов на 10 РПЗ (репрезентативных полей зрения), индекс пролиферации Ki-67 - 5% и более. Низкодифференцированные эндокринные карциномы по экспрессии гормонов и клинической симптоматике очень изменчивы, состоят из клеток мелких или средних размеров, растут в виде солидных пластов причудливой формы, часто с центральными некрозами и участками диффузного роста. Участки некроза выглядят как очаги размягчения желтоватой или «ржавой» окраски. Митотическая активность и индекс пролиферации обычно высокие (>10митозов на 10 РПЗ и >15% Ki-67- позитивных клеток), ядра крупные, полиморфные, с отчетливыми ядрышками. Для них характерны инвазия сосудов и нейроинвазия, массивное прорастание в окружающие органы и ткани, наличие отдаленных метастазов. Смешанные экзо-эндокринные карциномы - редкий тип опухолей, в которых и в первичной опухоли и в метастазах интимно связаны два компонента - протоко-вый и эндокринный, причем, эндокринный составляет не менее трети всей ткани опухоли. Прогноз для таких карцином значительно хуже, чем для большинства НЭО и определяется экзокринным компонентом опухоли.
Инсулиномы - инсулин-продуцирующие опухоли (рисунок, А, Б) составляют 70-75% всех функционирующих опухолей этого органа, чаще бывают спорадическими и встречаются у женщин в возрасте 30-60 лет, а в 4-10% возникают в рамках синдрома множественной эндокринной неоплазии 1 типа (МЭН-1, или синдром Вермера) [1, 2, 12]. Для инсулином характерен гипогликемический синдром, симптомы которого многообразны и зависят от целого ряда причин: размера опухоли, интенсивности секреции клетками инсулина, длительности заболевания, частоты приступов, индивидуальной чувствительности центральной нервной системы к снижению уровня глюкозы крови. В 1-5% случаев встречаются инсулиномы экстрапанкреатической локализации - в желудке, двенадцатиперстной, тощей, подвздошной кишке, желчном пузыре, малом сальнике и других органах.
Гастриномы. В 1955 г. Золлингером и Эллисоном был описан синдром (синдром Золлингера - Эллиссона (СЗЭ) с наличием характерного комплекса симптомов: тяжелой рецидивирующей язвенной болезни двенадцатиперстной кишки, гиперсекреторной активности слизистой желудка и эндокринных гастрин-продуцирующих опухолей (ПЖ или иной локализации). В ПЖ в 75% случаев опухоли локализуются в головке, растут хотя и медленно, но обладают более злокачественным потенциалом, чем дуоденальные, и могут давать метастазы в лимфатические узлы или печень. Размеры гастрином варьируют в широких пределах (от 0,4 до 15 см, в среднем 4 см), они чаще локализуются не в ПЖ, как считали раньше, а в двенадца-типерстной кишке (рисунок, В). Раньше при СЗЭ в 90% случаев применяли субтотальную гастрэктомию, а в последние десятилетия применение эффективных противоязвенных препаратов позволяет устранить симптомы эндокринной гиперфункции пациентов с гастриномами, но не устраняет саму причину [7]. Это привело к тому, что во всех индустриально развитых странах в последние годы возросла летальность, обусловленная прогрессированием не выявленных гастрином. Риск смерти у пациентов с гастриномами увеличивается при высоком уровне гастрина в сыворотке, крупных размерах опухоли и при ее локализации в ПЖ, при поздней диагностике и наличии метастазов в печень, кости или лимфатические узлы, при развитии у пациентов нескольких гиперфункциональных синдромов, особенно СЗЭ и синдрома Кушинга [6, 11, 12]. Гастриномы ПЖ чаще всего имеют трабекулярное или солидное, реже железистое строение. Иммунофенотип клеток гастрином характеризуется ко- экспрессией маркеров нейроэндокринной дифференцировки (хромогранина А, синаптофизина и CD56) и маркеров экзокринной дифференцировки (цитокератинов 19 и 20 и/или ЭМА), т.е. гастриномы ПЖ являются одновременно нейроэндокринными и экзокринными новообразованиями [1, 8].
Глюкагономы - это редкие, медленно растущие опухоли с неспецифическими симптомами, которые часто достигают крупных размеров и более чем в 50% случаев имеют плохой прогноз. Для синдрома глюкагономы (синдром Маллисона) характерны некротическая мигрирующая эритема, глоссит, хейлит, анемия, снижение массы тела, депрессия и венозный тромбоз. Первичные опухоли чаще локализуются в хвосте ПЖ. Обычно это солидные опухоли, клетки которых дают положительную реакцию с глюкагоном, интенсивность которой мало зависит от уровня гормона в сыворотке [1-3].
Соматостатиномы секретируют соматостатин, встречаются еще реже глюкагоном (до 1% всех НЭОПЖ), обычно имеют солидное строение. Для синдрома соматостатиномы характерны сахарный диабет, снижение массы тела, холелитиаз, стеаторея и гипохлоргидрия. Опухоли часто долго растут бессимптомно или со слабо выраженными неспецифическими симптомами, поэтому к моменту постановки диагноза большинство из них достигают больших размеров и дают метастазы в печень.
Нефункционирующие (или клинически «немые») опухоли (НФО) - это наиболее сложная для постановки диагноза группа НЭОПЖ. Они часто имеют ангиоматозное строение, и установить их нейроэндокринную дифференцировку часто удается только по положительной реакции мембраны опухолевых клеток с CD56, в то время как реакция с другими нейроэндокринными маркерами - синаптофизином и хромогранином А может быть очень слабой или отрицательной. Применение нескольких маркеров нейроэндокринной дифференцировки позволяет практически в 100% случаев поставить правильный диагноз НФО [1, 3].
Карциноиды ПЖ встречаются очень редко, их описано в литературе всего 100 случаев. Это злокачествен-ные опухоли, которые в 69-88,4% случаев дают метастазы и резистентны к терапии [10].
Синдром множественной эндокринной неоплазии 1 типа (МЭН-1) обусловлен мутацией в перицентрической области хромосомы 11 (11q13) и обычно наследуется по аутосомно-доминантному типу, реже является результатом новой мутации [13]. Мутация в области гена на 11q13 приводит к нерегулируемой пролиферации эндокринных клеток с поражением обязательной триады органов: это синхронное или асинхронное развитие гиперплазий и/или опухолей нескольких или всех 4 паращитовидных желез, эндокринных опухолей ПЖ и передней доли гипофиза. Реже одновременно возникают НЭО двенадцатиперстной кишки, желудка, еще реже - тимуса, легких, щитовидной железы, надпочечников [2,13,17]. Недавно показано, что при спорадических НЭОПЖ в 46% случаев также выявляют мутации на хромосоме 11q13 [17]. Хотя клинические проявления синдрома МЭН-1 очень вариабельны, но к 40-м годам практически у всех пациентов обязательно развиваются симптомы гиперпаратиреоза, а клиническая манифестация заболевания приходится на 3-4-ю декаду жизни [13]. Среди опухолей ПЖ при МЭН-1 преобладают клинически нефункционирующие [2], а из гиперфункциональных эндокринных синдромов - СЗЭ и гипогликемии (инсулиномы), реже - синдромы Вернера - Моррисона (ви- помы), глюкагономы, еще реже - синдромы Кушинга и акромегалии. Инсулиномы при МЭН-1 чаще множественные (в 40% их 5 и более) и более злокачественные, чем спорадические, а гастриномы, напротив, менее злокачественные. В ПЖ при МЭН-1 имеются множественные эндокринные микроаденомы, что может объяснить увеличение частоты рецидивов у таких пациентов (например, гипогликемического синдрома в 42%, по сравнению с 3% в спорадических случаях). Это требует особенно тщательного обследования пациентов с НЭОПЖ и проведения у них активного скрининга с целью выявления МЭН-1. Группой риска являются субъекты с первичным гиперпаратиреозом, опухолями ПЖ и гипофиза, синдромами гиперинсулинемии, СЗЭ и другими, а также с патологией сразу нескольких эндокринных органов, которая проявляется в возрасте до 50 лет. Обязательным является и тщательное изучение семейного анамнеза. Такая тактика позволяет поставить правильный диагноз у большинства пациентов даже без проведения у них кариотипирования [4, 8].
Основным фактором благоприятного прогноза при наличии у пациентов злокачественных НЭОПЖ является максимально радикальное их удаление, а неблагоприятного - наличие у них метастазов в печень, низкая степень дифференцировки опухолевых клеток и нерадикальное удаление опухоли [9-11, 14, 15]. Более 90% пациентов с доброкачественными НЭОПЖ и только 50% со злокачественными живут 5 и более лет [10, 15]. По нашим данным, злокачественным потенциалом обладают НЭОПЖ, для иммунофенотипа клеток которых характерна ко-экспрессия маркеров нейроэндокринной и экзокринной дифференцировки и/или нескольких гормонов одновременно [1, 2, 6].
Нейроэндокринные опухоли желудка (табл. 3) по разным данным, составляют 11-41% всех НЭОЖКТ. Их делят на 4 типа [16, 17].
1 тип, самый многочисленный, составляет до 70-80% всех случаев, из которых большинство (до 80%) - у женщин в возрасте 50-60 лет. Опухоли обычно не дают эндокринных синдромов и проявляются общими желудочными симптомами. Как правило, это небольшие округлые, полиповидные, мультифокальные образования, размером 0,5-1 см, чаще локализованные в теле желудка. Это обычно высокодифференцированные опухоли, локализованные в пределах слизистого или подслизистого слоев желудка и ассоциированные с хроническим атрофическим аутоиммунным гастритом. Они состоят из ECL-клеток, продуцирующих гистамин, которые дают интенсивную положительную реакцию с хромогранином А (рисунок, Г). Обычно у них прогноз хороший, так как это небольшие опухоли, которые могут быть удалены эндоскопически. Метастазы в регионарные лимфатические узлы могут давать опухоли размером более 2 см, которые инфильтрируют мышечную пластинку.
НЭО желудка 2 типа обычно возникают в рамках синдрома МЭН-1 и, как правило, ассоциированы с СЗЭ, встречается одинаково часто у женщин и мужчин в возрасте около 50 лет. Как и опухоли 1 типа, локализованы в теле желудка, имеют размеры менее 1,5 см, ограничены слизистым и подслизистым слоями, часто бывают множественными. В 10% случаев при наличии инвазии сосудов, размерах более 2 см и/или инвазии мышечной пластинки дают метастазы.
НЭО желудка 3 типа - это обычно спорадические солитарные опухоли, не ассоциированные ни с хроническим атрофическим гастритом, ни с МЭН-1, без преимущественной локализации. Это высокодифференци-рованные опухоли из ECL-клеток, серотонин- или гастрин-продуцирующих клеток, которые в трети случаев к моменту постановки диагноза имеют размеры более 2 см. В 70% случаев при опухолях размером более 2 см с инвазией сосудов и прорастанием мышечной пластинки имеются метастазы в лимфатические узлы.
НЭО желудка 4 типа соответствуют низкодифференцированным солидным карциномам из мелких или средних клеток (рисунок, Д), которые чаще встречаются у мужчин, очень редко ассоциированы с МЭН-1 (но не с хроническим атрофическим гастритом) и к моменту постановки диагноза обычно достигают крупных размеров (более 4 см) и дают обширные метастазы. Обычно клетки опухолей дают положительную реакцию с синптофизином, но отрицательны к хромогранину А. Прогноз неблагоприятный и примерно 2/3 пациентов умирают от метастазов в течение года с момента постановки диагноза.
Нейроэндокринные опухоли двенадцатиперстной и тощей кишки, по последним данным, составляют не менее 22% всех НЭОЖКТ, обычно протекают бессимптомно, чаще встречаются у мужчин возрасте 50-60 лет [4, 5, 9, 15, 16, 19].
Таблица №3.
Классификация эндокринных опухолей желудка [4, 19]
1. Высокодифференцированные опухоли - карциноиды
1.1. Доброкачественные: локализованы в пределах слизисго-подслизисгого слоя; без инвазии сосудов; размером < 1 см, нефункционирующие.
1.1.1. ECL-клеточные опухоли тела/фундального отдела с гипергастринемией и хроническим атрофическим гастритом или синдромом МЭН-1.
1.1.2. Серотонин-продуцирующие опухоли.
1.1.3. Гастрин-продуцирующие опухоли.
1.2. Опухоли неопределенной степени злокачественности: локализованы в пределах слизисто-подслизистого слоя; размером >1см или с инвазией сосудов.
1.2.1. ECL-клеточные опухоли с гипергастринемией и хроническим атрофическим гастритом, синдромом МЭН-1 или спорадические.
1.2.2. Серотонин-продуцирующие опухоли.
1.2.3. Гастрин-продуцирующие опухоли. |
2. Высокодифференцированные эндокринные карциномы: злокачественные карциноиды.
2.1. Низкой степени злокачественности, с глубокой инвазией (мышечной пластинки или более глубоких отделов) или с метастазами.
2.2. Нефункционирующие.
2.2.1. ECL-клеточные карциноиды, чаще спорадические, реже с гипергастринемией или на фоне синдрома МЭН-1.
2.2.2. Серотонин-продуцирующие опухоли.
2.2.3. Гастрин-продуцирующие опухоли.
2.3. Функционирующие.
2.3.1. ECL-клеточные карциноиды с атипичным карциноидным синдромом.
2.3.2. Серотонин-продуцирующие карциноиды с карциноидным синдромом.
2.3.3. Гастрин-продуцирующие карциномы - злокачественные гастриномы.
2.3.4. АКТГ-продуцирующие карциномы с синдромом Кушинга. |
| 3. Низкодифференцированные мелкоклеточные эндокринные карциномы высокой степени злокачественности, чаще нефункционирующие, иногда с синдромом Кушинга. |
Примечание: ECL - энтерохромаффинноподобные; МЭН-1 - синдром множественной эндокринной неоплазии 1 типа; а - <1 см доброкачественны почти в 100% случаев, а <2 см - почти в 80%.
В двенадцатиперстной и тощей кишках также выделяют 4 типа НЭО: гастриномы, соматостатиномы, нефункционирующие серотонин-, гастрин- или кальцитонин- продуцирующие низкодифференцированные нейроэндокринные карциномы и ганглиоцитарные параганглио- мы (табл. 4). Чаще всего (до 2/3 опухолей) встречаются гастриномы, затем соматостатиномы и НФО, а низкодифференцированные нейроэндокринные карциномы и ган- глиоцитарные параганглиомы - очень редкие и обычно локализованы в области Фатерова соска.
Дуоденальные гастриномы, ассоциированные с СЗЭ, бывают как спорадическими, так и в рамках МЭН-1, размером не более 1 см (рисунок, Г) и локализуются обычно в верхних отделах двенадцатиперстной кишки. Чаще всего имеют трабекулярное или железистое строение, дают положительную реакцию с гастрином, а в рамках синдрома МЭН-1 часто бывают множественными. Несмотря на небольшие размеры образований и то, что они ограничены слизистым или подслизистым слоями, в момент постановки диагноза они часто уже дают метастазы в регионарные лимфатические узлы, которые могут быть крупнее, чем первичная опухоль, поэтому их иногда ошибочно принимают за первичные гастриномы ПЖ и даже лимфатических узлов. По этой же причине раньше выявляли значительно больше гастрином ПЖ, чем в настоящее время. Метастазы в регионарные лимфатические узлы дуоденальные гастриномы могут давать уже на ранних стадиях, а метастазы в печень, в отличие от гаст- рином ПЖ - значительно позже.
Дуоденальные соматостатиномы составляют до 20% всех НЭО этой локализации, чаще встречаются в Фате- ровом соске. Имеют часто железистое строение с наличием псаммомных телец, их клетки обычно дают положительную реакцию с соматостатином. При инвазии опухолью мышечной пластинки вероятность наличия метастазов в парадуоденальные лимфатические узлы очень велика. Опухоли обычно не дают специфического синдрома соматостатиномы (диабета, холелитиаза или диареи), но иногда ассоциированы с нейрофиброматозом 1 типа и с билатеральными феохромоцитомами.
Нефункционирующие дуоденальные НЭО обычно состоят из серотонин-, реже - из гастрин- и кальцитонин- продуцирующих клеток. Для них прогноз лучше, чем для СЗЭ-ассоциированных гастрином или соматостатином Фатерова соска. Если опухоли не прорастают подслизистый слой, они обычно не дают метастазов.
Низкодифференцированные дуоденальные карциномы обычно гормонально не активны и возникают в области Фатерова соска. Это мелкоклеточные карциномы из недифференцированных клеток, которые в момент постановки диагноза уже обычно метастазируют в регионарные лимфатические узлы и печень, дают интенсивную реакцию с синаптофизином и очень слабую или отрицательную - с хромогранином А.
Дуоденальные ганглиоцитарные параганглиомы локализуются вблизи Фатерова соска и обычно доброкаче-ственные, даже если они по размеру превышают 2 см и прорастают мышечную пластинку. Состоят из ганглио- цитарных и высокодифференцированных нейроэндокринных клеток, которые дают положительную реакцию с соматостатином, панкреатическим полипептидом и протеином S-100.
Нейроэндокринные опухоли дистального отдела тощей и подвздошной кишок (табл. 5) составляют около 25% всех НЭОЖКТ и вместе с соответствующими опухолями желудка и аппендикса являются самой многочисленной группой [4, 15, 16, 19]. Чаще всего встречаются в возрасте около 60 лет, одинаково часто у мужчин и у женщин. Обычно опухоли имеют альвеолярно-солидное строение, к моменту постановки диагноза имеют размеры более 2 см, прорастают мышечную пластинку (рисунок, Ж, З) и дают метастазы в регионарные лимфатические узлы. Примерно в 40% случаев опухоли бывают множественными, состоят из серотонин-, субстанцию Р-, каликреин-, катехоламин-продуцирующих и других типов клеток. У 20% пациентов с НЭО подвздошной кишки развивается типичный карциноидный синдром и имеются метастазы в регионарные лимфатические узлы и печень. Агрессивные низкодифференцированные НЭО в подвздошной кишке не описаны.
Таблица №4.
Классификация эндокринных опухолей двенадцатиперстной и верхних отделов тощей кишки [4, 19]
1. Высокодифференцированные опухоли - карциноиды.
1.1. Доброкачественные: нефункционирующие, локализованные в пределах слизисто-подслизисгого слоя; размером <1 см; без инвазии сосудов.
1.1.1. Гастрин-продуцирующие опухоли (проксимальный отдел двенадцатиперстной кишки).
1.1.2. Серотонин-продуцирующие опухоли.
1.1.3. Ганглиоцитарные параганглиомы, независимо от размеров (в области Фатерова соска).
1.2. Опухоли неопределенной степени злокачественности: локализованы в пределах слизисто-подслизистого слоя; размером >1см или с инвазией сосудов.
1.2.1. Гастрин-продуцирующие опухоли, функционирующие (гастриномы) или нефункционирующие, спорадические или МЭН-1- ассоциированные.
1.2.2. Соматостатин-продуцирующие опухоли (в области Фатерова соска, ассоциированные или нет с болезнью Реклингаузена).
1.2.3. Серотонин-продуцирующие опухоли, нефункционирующие.
1.2.3. Гастрин-продуцирующие опухоли. |
2. Высокодифференцированные эндокринные карциномы: злокачественные карциноиды.
2.1. Низкой степени злокачественности, с глубокой инвазией подслизистой или с метастазами.
2.2. Гастрин-продуцирующие карциномы функционирующие (гастриномы) или нефункционирующие, спорадические или МЭН-1-ассоциированные.
2.3. Соматостатин-продуцирующие карциномы (в области Фатерова соска, ассоциированные с болезнью Реклингаузена или без нее).
2.4. Серотонин-продуцирующие карциномы, функционирующие или нефункционирующие (независимо от размеров и распространенности) с карциноидным синдромом.
2.5. Злокачественные ганглиоцитарные параганглиомы
2.2.3. Гастрин-продуцирующие опухоли. |
| 3. Низкодифференцированные мелкоклеточные эндокринные карциномы высокой степени злокачественности. |
| 4. Опухоли высокой степени злокачественности (в области Фатерова соска). |
Нейроэндокринные опухоли толстой и прямой кишки (табл. 6). В то время как НЭО толстой кишки встречаются редко (рисунок Е., И), в прямой кишке они составляют почти 20% всех НЭОЖКТ (табл. 5). НЭО толстой кишки - это чаще всего низкодифференцированные карциномы, которые к моменту постановки диагноза уже дают метастазы и имеют плохой прогноз (рисунок, И). В опухолях часто выявляются небольшое число рассеянных серотонин- и соматостатин-позитивных клеток.
НЭО прямой кишки встречаются чаще и имеют более благоприятный прогноз. Большинство из них выявляют эндоскопически как маленькие образования (<1 см), расположенные в подслизистом слое, клетки которых часто дают положительную реакцию с глюкагоном, глицети- ном и/или панкреатическим полипептидом. Метастази- руют только опухоли размером более 2 см и/или, если они прорастают мышечную пластинку. В этом отделе кишечника низкодифференцированные нейроэндокринные карциномы встречаются крайне редко и имеют исключительно плохой прогноз.
Нейроэндокринные опухоли аппендикса составляют до 20% всех НЭОЖКТ (табл. 6) и в отличие от других, встречаются в более молодой возрастной группе (30-50 лет), чаще у женщин, а в редких случаях - у детей. Как правило, их обнаруживают при аппендэктомии, в основном они локализуются в верхних отделах аппендикса, почти всегда прорастают мышечную пластинку и в различной степени окружающую жировую клетчатку. Опухоли редко бывают более 2,5 см, редко дают метастазы в лимфатические узлы, и имеют более благоприятный прогноз, чем НЭО подвздошной кишки. НЭО аппендикса напоминают соответствующие опухоли тощей кишки: обычно имеют альвеолярно-солидное строение, их клетки часто позитивны к серотонину и субстанции Р, значительно реже - к энтероглюкагону. Серотонин-продуци- рующие опухоли аппендикса обычно не метастазируют в печень и очень редко дают карциноидный синдром. Эти НЭО следует дифференцировать с очень редкими бокаловидно-клеточными карциноидами, которые являются смешанными экзо-эндокринными опухолями с менее благоприятным прогнозом.
У 13% пациентов встречается сочетание синхронных и метахронных аденокарцином и НЭОЖКТ [10]. В частности, аденокарциномы и мелкоклеточные эндокринные карциномы описаны в толстой кишке, аппендиксе [17], а, по нашим данным, они встречаются и в желудке.
Таблица №5.
Классификация эндокринных опухолей подвздошной, слепой, толстой и прямой кишки [4,19]
1. Высокодифференцированные опухоли - карциноиды.
1.1. Доброкачественные: нефункционирующие, локализованы в пределах слизисто- подслизистого слоя; без инвазии сосудов; размером <1 см (тонкая кишка) или <2 см (толстая кишка).
1.1.1. Серотонин-продуцирующие опухоли.
1.1.2. Энтероглюкагон-продуцирующие опухоли.
1.2. Опухоли неопределенной степени злокачественности: локализованы в пределах слизисто-подслизистого слоя; размером 21см (тонкая кишка) или 22 см (толстая кишка) или с инвазией сосудов.
1.2.1. Серотонин-продуцирующие опухоли. |
2. Высокодифференцированные эндокринные карциномы: карциноиды низкой степени злокачественности, с глубокой инвазией (мышечной пластинки и более глубоких отделов) или с метастазами.
2.1. Серотонин-продуцирующие карциноиды с карциноидным синдромом или без него.
2.2. Энтероглюкагон-продуцирующие карциномы. |
| 3. Низкодифференцированные эндокринные мелкоклеточные карциномы высокой степени злокачественности. |
| 4. Смешанные экзо-эндокринные карциномы умеренной или высокой степени злокачественности. |
Таблица №6.
Классификация эндокринных опухолей аппендикса [4, 19]
1. Высокодифференцированные эндокринные опухоли – доброкачественные нефункционирующие карциноиды с инвазией стенки, без инвазии сосудов, размером J2 см.
1.1. Серотонин-продуцирующие опухоли.
1.2. Энтероглюкагон-продуцирующие опухоли неопределенной степени злокачественности, нефункционирующие, с инвазией подслизистого слоя; размером 22 см или с инвазией сосудов.
|
2. Высокодифференцированные эндокринные карциномы – злокачественные карциноиды.
2.1. Серотонин-продуцирующие карциноиды с карциноидным синдромом или без него.
2.2. Опухоли низкой степени злокачественности с инвазией средних или более глубоких отделов и/или с метастазами. |
3. Смешанные экзо-эндокринные карциномы.
3.1. Низкой степени злокачественности – бокаловидно-клеточные карциноиды. |
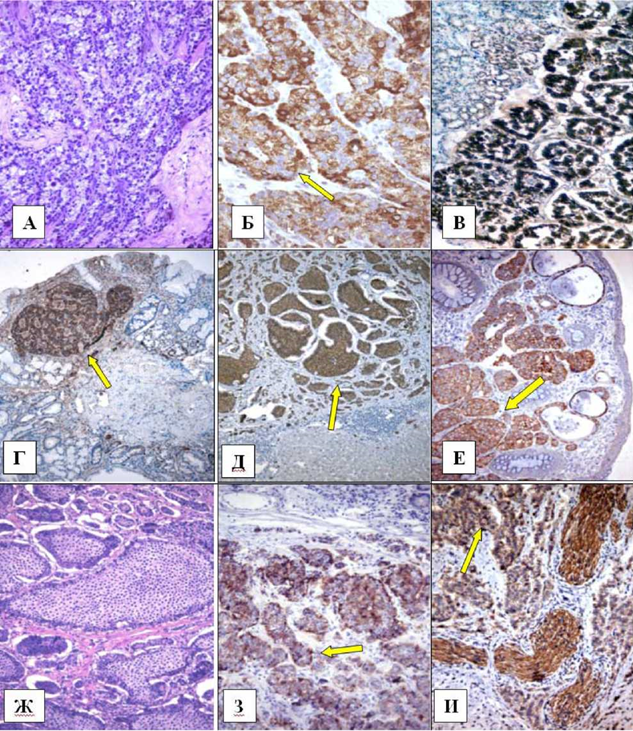
А, Б – инсулинома поджелудочной железы. Реакция клеток опухоли с инсулином (Б) Ув. х250. В – гастринома двенадцатиперстной кишки. Реакция с гастрином Ув. х250. Г – Нейроэндокринная опухоль желудка. Реакция с синаптофизином. Ув. х125. Д – метастаз злокачественной нефункционирующей нейроэндокринной опухоли тела желудка в печень. Реакция с хромогранином А. Ув. х125. Е – нейроэндокринная опухоль толстой кишки с очаговым прорастанием мышечной пластинки слизистой оболочки. Реакция с синаптофизином. Ув. х125. Ж, З – карциноид тонкой кишки альвеолярно5 солидного строения. Реакция с серотонином (З). Ув. х125, 250. И – злокачественная нейроэндокринная опухоль прямой кишки, инфильтрирующая слизистый и мышечный слои. Реакция с CD56. Ув. х 250. А, Ж – окраска гематоксилином и эозином. Б–Е, З, И – иммуногистохимическая реакция. ПАП5метод, докраска ядер гематоксилином Майера.
Большинство НЭОЖКТ - это нефункционирующие опухоли, клетки которых продуцируют пептиды и/или амины, которые не дают типичных эндокринных синдромов, поэтому их реальное количество и распространенность определить трудно. В то же время, их клетки реализуют в кровеносное русло хромогранин А - пептид, увеличение уровня которого в сыворотке в на-стоящее время используют для прогнозирования наличия метастазов у пациентов с НЭО, но при небольших размерах опухоли он часто бывает в пределах нормы.
Литература
1. Гуревич ЛЕ. Иммуногистохимическая диагностика опухолей поджелудочной железы // Иммуногистохимичес- кая диагностика опухолей человека / Под ред. Н.Т. Райхлина, С.В. Петрова. Гл. 7. - Казань, 2004. - С. 76-92.
2. Казанцева ИА., Гуревич ЛЕ. Роль полипотентных клеток в развитии опухолей поджелудочной железы // Арх. пат. в печати.
3. Кузин НМ, Егоров АВ. Нейроэндокринные опухоли поджелудочной железы. - М.: Медицина, 2001.
4. Arnold R. Introduction: definition, historical aspects, classification, staging, prognosis and therapeutic options // Best Pract. & Res. Clin. Gastroenterol. - 2005. - Vol. 19, №4 - Р. 491-505.
5. Bornstein-Quevedo, Gamboa-Dominguez A. Carcinoid tumors of the duodenum and ampulla of Vater: a clinicomorphologic, immunohistochemical and cell kinetic comparison // Hum. Pathol. - 2001. - Vol. 32. - P. 1252-1256.
6. Deshapande V., Selig MK, Nielsen G.P. et al. Ductulo-insular pancreatic endocrine neoplasms: clinicopathologic analysis of a unique subtype of pancreatic endocrine neoplasms // Amer. J. Surg. Pathol. - 2003. - Vol. 27, №4. - P. 461-468.
7. Ellison E.ch, Sparks J. Zollinger-Ellison syndrome in era of effective acid suppression: are we unknowingly growing tumors? // Amer. J. Surg. - 2003. - Vol. 186. - P. 245-248.
8. Gurevich L, Kazantseva I, Isakov V. et al. The analysis of immunophenotype of gastrin-producing tumors of pancreas and gastrointestinal tract // Cancer. - 2003. - Vol. 98, №9. - Р . 1967-1976.
9. Jorda M, Gorab Z., Fernandes G. et al. Low nuclear proliferative activity is associated with nonmetastatic islet cell tumors // Arch. Pathol. Lab. Med. - 2003. - Vol. 127. - P. 196-199.
10. Kalt GA, Besser GM, Grossman AB. The diagnosis and medical management of advanced neuroendocrine tumors // End. Reviews. - 2004. - Vol. 25(3). - P. 458-511.
11. Kloppel G, Anlauf M. Epidemiology, tumor biology and histopathological classification of neuroendocrine tumours of the gastrointestinal tract // Best. Pract. & Res. Clin. Gastroenterol. - 2005. - Vol. 19, №4. - P. 507-517.
12. Madeira I, Terris B, Voss M. et al. Prognostic factors in patients with endocrine tumors of the duodenopancreatic area // Gut. - 1998. - Vol. 43. - P. 422-427.
13. Padberg B, Schroder S., Capella C. et al. Multiple endocrine neoplasia type-1 (MEN-1) revisited // Virch. Arch. - 1995. - Vol. 426. - P. 541-548.
14. Phan G.Q., Yeo C.J, Hruban RH. et al. Surgical experience with pancreatic and peripancreatic neuroendocrine tumors: review of 125 patients // J. Gastrointest. Surg. - 1998. - Vol. 2. - P. 473-482.
15. Plockinger U, Wiedenmann B. Management of metastatic endocrine tumors // Best. Pract. & Res. Clin. Gastroenterol. - 2005. - Vol. 19, №4. - P. 553-576.
16. Rindi G, Ubiali A., Villanacci V. The phenotype of gut endocrine tumors // Digestive& Liver Disease 36 (Suppl. 1). - 2004. - S 26-30.
17. Rindi G, Bordi C. Etiology, molecular pathogenesis and genetics // Best. Pract. & Res. Clin. Gastroenterol. - 2005. - Vol. 19, №4. - P. 519-534.
18. Solcia E, Capella C, Kloppel G. Tumors of the Pancreas // Atlas of Tumor Pathology. Third Series, Fasc. 20. - Bethesda: Marylend, 1997.
19. Solcia E, Kloppel G, Sobin LH World Health Organization: International Histological Classification of Tumors: Histological Typing of Endocrine Tumors. - Berlin: Springer, 2000.
20 SchusslerMH, SkoudyA., Ramaekers F. et al. Intermediate filaments as differentiation markers of normal pancreate and pancreas cancer // Amer. J. Pathol. - 1992. - Vol. 140. - P. 559-568.
21. Van Eeden S., Quaedvlieg PFH.J, Taal B.G. et al. Classication of low-grade neuroendocrine tumors midgut and unknown origin // Hum. Pathol. - 2002. - Vol. 33. - P. 1126-1132.


